类风湿关节炎新突破:难治性疾病诊断、治疗策略变化与精准检测进展 | EULAR 2025
丁香园编辑团队已抵达大会现场,为您带来风湿病学领域第一手学术资讯~
✦
类风湿关节炎(RA)是一种系统性自身免疫性疾病,主要特征是慢性炎症性关节病变,常累及手、足小关节,表现为对称性、持续性关节肿胀和疼痛。除关节症状外,RA 还可能引发心脏、肺部、神经系统等多系统的并发症,严重影响患者生活质量[1]。
✦
2025 年 6 月 11 日至 14 日,一年一度的欧洲风湿病学大会(EULAR 2025)将在西班牙巴塞罗那隆重举行。RA 作为常见风湿病,在本届大会上公布了多项值得关注的进展,本文将整理部分 RA 领域的亮点研究,以飨读者。
POS0028:MSUS 或可用于检测难治性 RA[2]
研究目的:探讨肌骨超声(MSUS)在难治性类风湿关节炎(Difficult-to-Treat RA,D2T-RA)患者中的应用价值,特别是其在识别关节炎特征和指导疾病分型方面的作用。

图 1:POS0028 摘要截图
研究背景:部分 D2T-RA 患者在接受多种先进抗风湿药物治疗后,仍表现出持续的疾病活动。近年来,研究者提出可将 D2T-RA 分为两种亚型:持续性炎症难治型(PIRRA)和非炎症难治型(NIRRA)。虽然这两种类型并不完全相互排斥,但 MSUS 作为一种敏感的影像学工具,可辅助识别未被临床发现的炎症。然而,目前尚不清楚 MSUS 在 D2T-RA 患者中所表现出的具体炎症特征,包括受累关节的分布及其在单个关节内的炎症部位,同时也不清楚其是否能够通过检测亚临床炎症来减少 NIRRA 的判定比例。
研究方法:回顾 2018 至 2024 年间在庆应大学医院就诊、符合 D2T-RA 定义的所有连续患者。若在临床存在肿胀的关节中,MSUS 检测出滑膜炎、腱鞘炎或腱周炎(PD 信号 ≥ 1 级),则定义为 PIRRA;若无此类炎症表现,则为 NIRRA。若患者无临床肿胀关节,但 MSUS 检测出上述炎症表现,则归类为「亚临床PIRRA」。所有数据分析均使用 JMP 版本 17 完成。
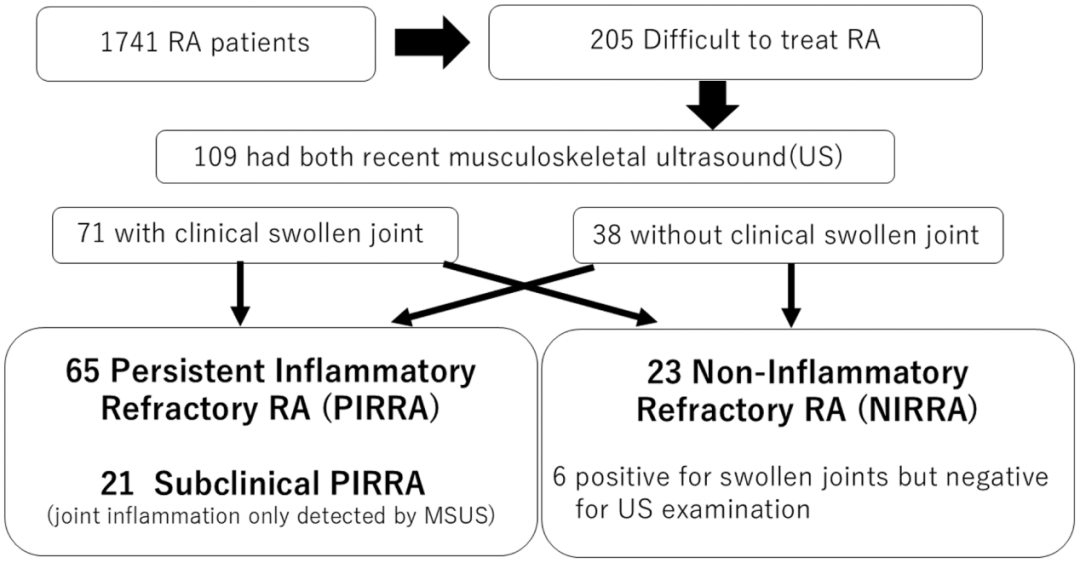
图 2:POS0028 研究方法示意图
研究结果:在 1,741 例 RA 患者中,205 例(11.8%)被认定为 D2T-RA,其中 109 例接受了 MSUS 检查。65 例(59.6%)被归类为 PIRRA。在 38 例无临床肿胀关节的患者中,有 21 例(19.3%)因 MSUS 检测出亚临床炎症而由 NIRRA 重新归类为亚临床 PIRRA。PIRRA 患者中,手腕是最常见的炎症部位,MSUS 检出率为 56.9%,显著高于临床检查的 38.4%(p = 0.01),该差异主要来自 MSUS 对腱结构炎症的识别。此外,踝关节和足部的 MSUS 炎症在亚临床 PIRRA 患者中较为常见(n = 9,占 42.9%)。进一步分析发现,MSUS 残留炎症的部位显著关联于最初临床滑膜炎的发生部位(p = 0.017)以及 RA 诊断时影像学所见的骨侵蚀关节(p < 0.001)。
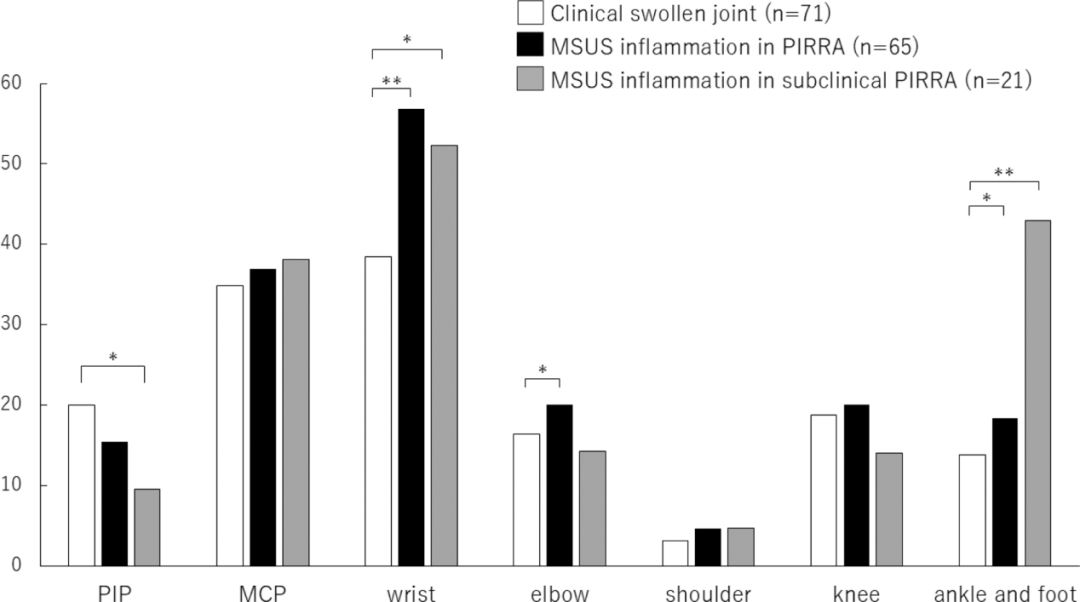
图 3:不同身体部位关节肿胀和 MSUS 检测到炎症情况
研究结论:MSUS 是一种对 D2T-RA 炎症检测极具价值的工具,尤其在无临床滑膜炎表现的患者中,可识别潜在的亚临床炎症。踝关节与足部为亚临床炎症的高发部位,而初诊时的临床滑膜炎及骨侵蚀部位可作为预测后续持续性关节炎的重要指标。
POS0151 :控制 RA 疾病活动度或可降低并发症风险[3]
研究目的:基于乌帕替尼(UPA)治疗类风湿关节炎(RA)的大型 Ⅲ 期临床试验(SELECT 系列临床试验)进行整合性事后分析,旨在探讨疾病活动度与不良事件(AEs)发生风险之间的关系。

图 4:POS0151 摘要截图
研究背景:RA 患者罹患主要心血管事件(MACE)、静脉血栓栓塞(VTE)及严重感染(SIE)的风险升高。目前关于有效控制疾病活动是否能降低这些不良事件发生率的证据仍有限。
研究方法:本分析整合了 6 项 Ⅲ 期 SELECT 系列临床试验数据,纳入所有接受过至少一次 Upadacitinib(UPA)15 mg 治疗,且起始时临床疾病活动指数(CDAI)评分 > 10 的患者。数据分析最长至 5 年(260 周),其中 SELECT-CHOICE 仅至 4.2 年(216 周)。采用 Cox 回归分析,以 CDAI 疾病活动分级(缓解、低、中、高)及高敏 C 反应蛋白(hsCRP)水平为时间依赖变量,并调整文献中已知的混杂因素。另以协方差分析(ANCOVA)比较有无不良事件患者的平均 CDAI。
研究结果:
共纳入 2623 名每日接受 15 mg Upadacitinib 治疗的类风湿关节炎患者。至平均随访 4.2 年时(为 6 项临床试验中所有数据可获得的最晚时间点),共有 43% 的患者(723 人)达到 CDAI 缓解状态,40%(660 人)处于低疾病活动度(LDA),14%(240人)为中度活动(MDA),仅 3%(43人)仍处于高疾病活动度(HDA)。
Cox 回归分析显示,相比达成缓解患者,处于 CDAI 高疾病活动度的患者在五年内发生 MACE 和 VTE 的风险显著升高。具体而言,MACE 的风险增加约 4.5 倍(HR 4.5,95% CI:1.3~15.4,P < 0.05),VTE 的风险则提高约 5.7 倍(HR 5.7,95% CI:1.8~18.2,P < 0.01)。
炎症水平指标方面,hsCRP 每升高 5 mg/L,MACE、VTE 和 SIE 的风险分别增加 7.1%~7.5%,而带状疱疹的风险也上升了 4.4%。进一步的分析发现,发生 VTE 的患者其时间加权平均 CDAI 分数较未发生者高出 4.2 分(P < 0.05)。
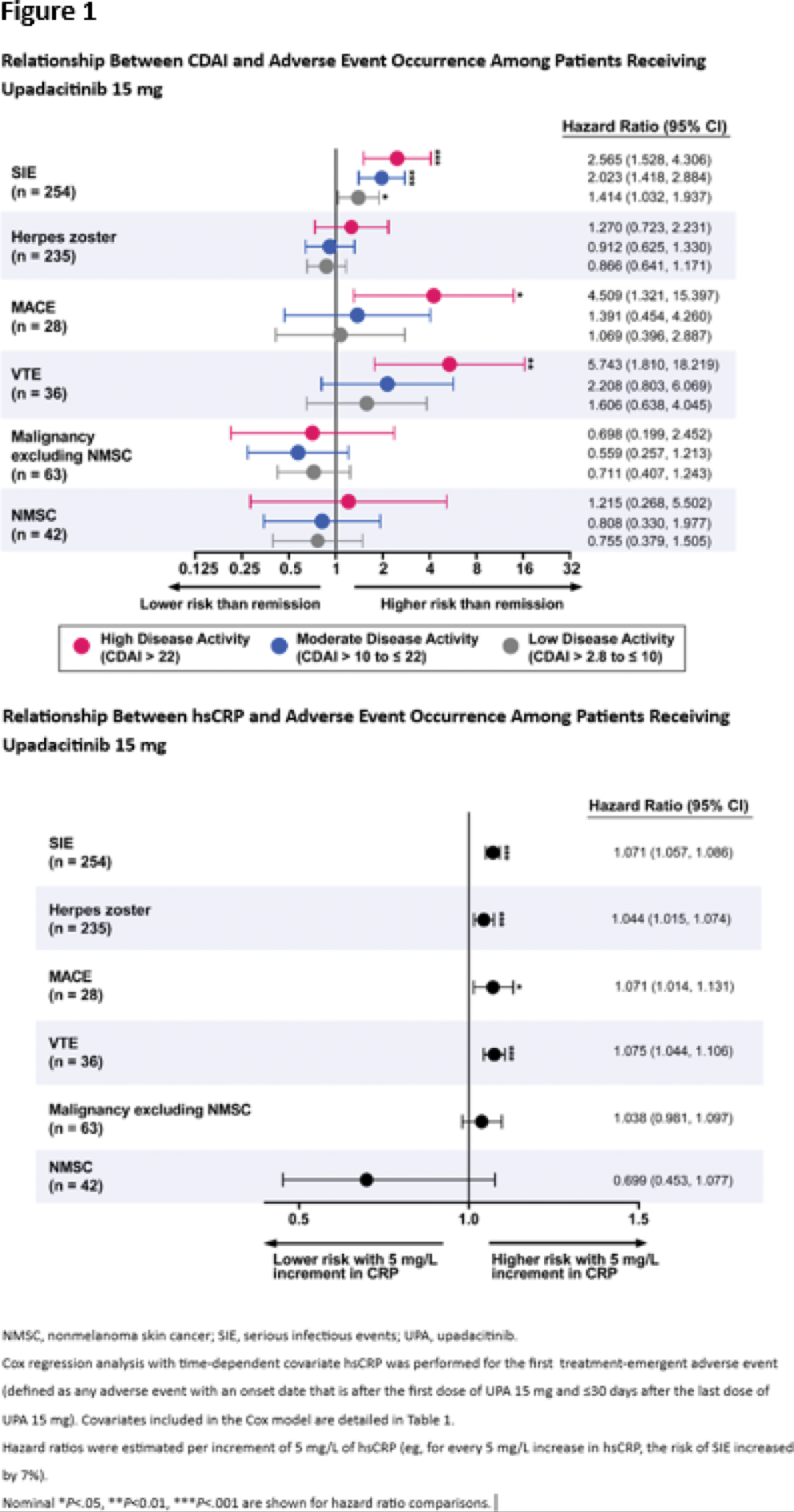
图 5:CDAI/hsCRP 与不良事件发生率的关系
研究结论:在 UPA 15 mg 治疗 RA 患者中,缓解状态者较高疾病活动度者 MACE、VTE 及 SIE 发生风险显著减少,表明积极控制炎症、实现临床缓解有助于降低部分严重不良事件的发生风险。
POS0751:JAKi 治疗失败后如何进行药物选择?[4]
研究目的:本研究旨在探讨 RA 患者在停用 JAKi 后改用不同靶向治疗方案,其临床反应是否存在差异。

图 6:POS0751 摘要截图
研究背景:靶向合成抗风湿药物(tsDMARDs)是类风湿关节炎(RA)治疗中的一类重要药物。然而,当前尚不明确在 Janus 激酶抑制剂(JAKi)停用后,应选择哪类生物制剂(bDMARD)或作用机制更为合适。
研究方法:研究基于比利时 TARDIS 电子数据库,纳入曾使用 JAKi 后停药并改用其他靶向治疗的 RA 患者。治疗方案分为肿瘤坏死因子抑制剂(TNFi)、T/B 细胞靶向治疗(主要为 Abatacept)、白介素(IL)-6 抑制剂(IL-6i)及再次使用 JAKi 四组,比较四组患者在 3~6 个月、15~18 个月和 27~30 个月时的关节疾病活动度 28 项(DAS28)评分改善与缓解率(DAS28 < 2.6)差异。应用混合效应模型进行统计分析,控制患者个体差异与重复测量偏倚。
研究结果:共纳入 2,389 例停用 JAKi 的 RA 患者,其中分别有 34%(821 人)使用 TNFi、18%(437 人)使用 T/B 细胞治疗、18%(423 人)使用 IL-6i、30%(708 人)重新使用 JAKi。在有随访数据的 1,274 例患者中,因比利时的报销规定,利妥昔单抗使用者(仅在病情复发时记录)被排除,T/B 细胞组最终仅包含 Abatacept 治疗者。为排除非医疗原因的换药,进一步排除基线缓解的患者(tsDMARD 组 12%,bDMARD 组 5%~6%)。最终纳入 1,190 例患者用于分析。具体结果如下:
缓解率比较:第一次随访(3~6 个月):Abatacept 组缓解率显著低于其他组(p = 0.008);后两次随访(15~18 个月,27~30 个月):差异不再显著(p = 0.268,p = 0.135),可能受「健康幸存者偏倚」影响。
各治疗线中,Abatacept 的缓解率普遍低于其他治疗组。
调整变量(包括控制基线病程、ESR、CRP、PGA、SJC28、TJC28)后, Abatacept 仍表现较差(−0.299,95% CI:−0.499 至 −0.003,p = 0.021)
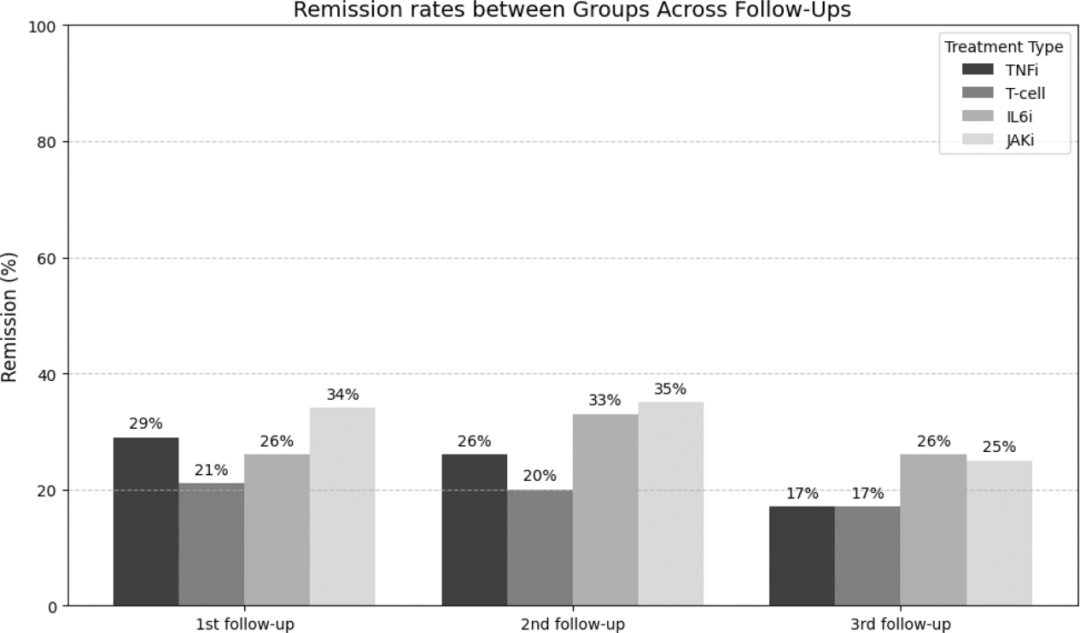
图 7:每组患者在不同随访时间点的缓解率
研究结论:在首次 JAKi 治疗失败后,RA 患者改用 TNFi、IL-6i 或重新使用 JAKi 均可获得令人满意的疗效;然而,在许多情况下,Abatacept 似乎并非理想的选择。尽管如此,为了充分验证以上结论,有必要对既往接受过新疗法的患者进行全面评估。
POS0032:IL-6i 治疗失败后,有何新选择?[5]
研究目的:评估在类风湿关节炎(RA)患者中,从 IL-6i(一线 bDMARD)换用其他靶向分子治疗的疗效。

图 8:POS0032 摘要截图
研究背景:2022 年 EULAR 指南更新建议,在生物制剂(bDMARDs)或靶向合成抗风湿药物(tsDMARDs)治疗失败后,应考虑更换为其他靶向药物。然而,关于 IL-6i 治疗无效后的换药策略,尤其是换用其他靶向药物的有效性仍没有得到充分讨论。
研究方法:利用大阪公立大学数据库中 1,600 余例接受靶向治疗的 RA 患者资料,筛选出以 IL-6i 为一期治疗并进入三期治疗的患者,分析其 52 周的药物持续率及 CDAI 评分变化,治疗药物包括 TNFi、其他 IL-6i、CTLA4-Ig(主要为 Abatacept)和 JAKi。
研究结果:TNFi 组的 52 周药物持续治疗率最高,达到 91.7%(11/12)。CTLA4-Ig 组的持续率为 75.0%(3/4),略低于 TNFi,但与其差异无统计学意义(p = 0.383)。相比之下,JAKi 和再次使用 IL-6i 的持续率明显较低,分别为 37.5%(3/8)和 16.7%(1/6),与 TNFi 组相比均具有统计学差异(p < 0.01)。对于完成 52 周治疗的患者,TNFi 组的 CDAI 由平均 18.7 显著下降至 7.7,显示出良好的疾病控制;CTLA4-Ig 组 CDAI 由 20.0 降至 9.9,同样表现出明显疗效。JAKi 组 CDAI 由 26.5 降至 12.2,虽有改善,但起始疾病活动度较高,整体疗效相对有限。而再次使用 IL-6i 的患者 CDAI 几乎无变化,仅由 22.4 轻微降至 22.3,提示治疗效果不佳。
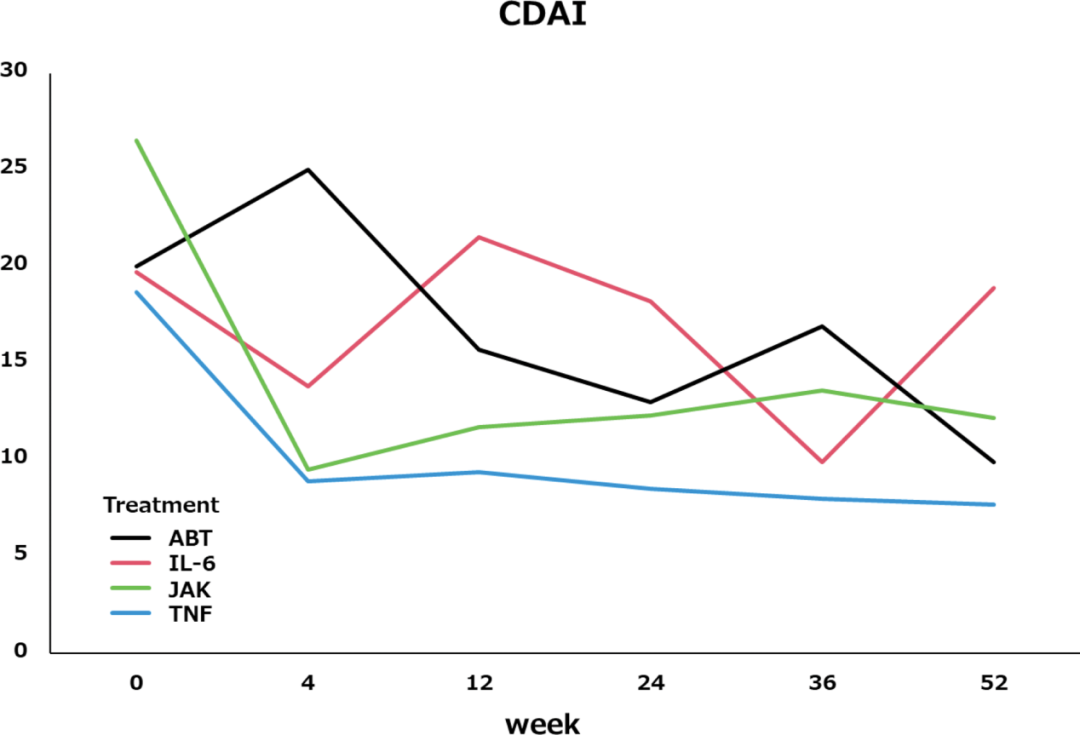
图 9:52 周期间 CDAI 评分变化
研究结论:IL-6i 治疗失败的 RA 患者,应优先考虑作用机制不同的靶向药物。TNFi 和 CTLA4-Ig 在药物持续率和疗效方面表现更优,而 JAKi 在这种情况下获益可能有限。
小结
在 2025 年 EULAR 大会上公布的多项研究摘要为 RA 的诊断和治疗提供了新见解。其中,MSUS 在检测难治性 RA 的亚临床炎症方面具有潜力,有助于更精准的疾病分型;SELECT 系列研究的事后分析显示,控制 RA 疾病活动度或有助于降低严重不良事件风险;此外,针对 JAKi 和 IL-6i 治疗失败后的 RA 患者,新的研究数据指出了后线治疗的方向。
✩ 本文仅供医疗卫生等专业人士参考
投稿邮箱:huanghaihua@dxy.cn
策划:Marina
参考文献:
[1] Radu, A. F., & Bungau, S. G. (2021). Management of Rheumatoid Arthritis: An Overview. Cells, 10(11), 2857. https://doi.org/10.3390/cells10112857
[2] Y. Kondo, et al. Characteristics and Impact of Joint Inflammation Detected by Musculoskeletal Ultrasound in Patients with Difficult-to-Treat Rheumatoid Arthritis. EULAR 2025, Abstract#POS0028.
[3] R. Fleischmann, et al. RELATIONSHIP BETWEEN DISEASE ACTIVITY AND ADVERSE EVENTS IN RHEUMATOID ARTHRITIS: AN INTEGRATED POST HOC ANALYSIS OF UPADACITINIB PHASE 3 TRIALS.EULAR 2025, Abstract#POS0151.
[4] D. De Cock, et al. OPTIMAL TREATMENT STRATEGIES FOLLOWING JAKi DISCONTINUATION IN RHEUMATOID ARTHRITIS.EULAR 2025, Abstract#POS0751.
